的反应历程示意图如下。下列说法正确的是
的反应历程示意图如下。下列说法正确的是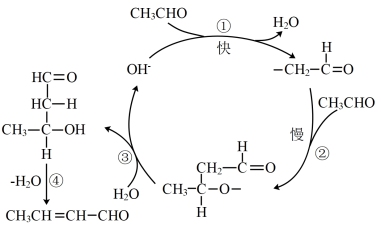
| A.苯甲醛也能发生类似反应 |
| B.反应①的活化能大于反应②的活化能 |
C.反应中,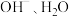 均为反应催化剂 均为反应催化剂 |
D.由上述历程可知醛基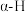 的酸性强于醇羟基 的酸性强于醇羟基 |
相似题推荐
| A.需要持续不断加热才能发生的反应一定是吸热反应 |
| B.化学键的断裂和形成是化学反应中能量变化的根本原因 |
| C.因为石墨变成金刚石吸热,所以石墨比金刚石稳定 |
| D.燃料电池是一种高效且对环境友好的新型电池 |

| A.在Sn-Ni合金催化下,该历程中最大能垒(活化能)为3.809eV•mol-1 |
| B.在Sn-Ni合金催化下,第二个反应阶段的化学方程式为CH3*+H*→CH2*+2H* |
| C.在Pt-Ni合金催化下,甲烷脱氢反应分为3个基元反应阶段 |
| D.两种催化剂比较,脱氢反应阶段催化效果更好的是Pt-Ni合金 |

| A.H2(g)转化为氢原子是一个放热过程 |
| B.1molH2和1molCl2的总能量比2molHCl的总能量低 |
| C.1 个 HCl(g)分子中的化学键断裂时需要吸收431.8 kJ能量 |
| D.2HCl(g)= H2(g)+Cl2(g)的反应热ΔH=+184.5 kJ·mol-1 |

| A.N4的熔点比 P4高 | B.1 mol N4气体转化为 N2时要吸收 724 kJ 能量 |
| C.N4与 N2互为同位素 | D.1 mol N4气体转化为 N2时要放出 724 kJ 能量 |
 N放出942 kJ热量。根据以上信息和数据,判断下列说法正确的是( )
N放出942 kJ热量。根据以上信息和数据,判断下列说法正确的是( )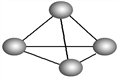
| A.N4属于一种新型的化合物 | B.N4分子中存在非极性键 |
| C.N4和N2是同分异构体 | D.1 mol N4转变成N2将吸收882 kJ热量 |

下列有关说法正确的是
| A.状态Ⅰ中产生了活性的氢分子 |
| B.由原料到状态Ⅰ吸收能量 |
| C.总反应过程中没有涉及氧化还原反应 |
D.总反应的化学方程式为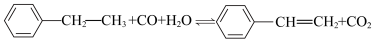 |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有2mL 溶液的试管中滴加1mL 溶液的试管中滴加1mL NaCl溶液,再向其中滴加4~5滴 NaCl溶液,再向其中滴加4~5滴 KI溶液 KI溶液 | 先有白色沉淀生成,后又产生黄色沉淀 |  |
| B | 向等浓度等体积的 中分别加入等浓度等体积的 中分别加入等浓度等体积的 溶液和 溶液和 溶液 溶液 | 前者产生气泡速率快 |  的催化效果比 的催化效果比 好 好 |
| C | 将银粉加到HI溶液中 | 产生无色气体和黄色沉淀 |  和 和 形成沉淀,促进Ag和 形成沉淀,促进Ag和 反应 反应 |
| D | 用铂电极电解等物质的量浓度的 和 和 混合溶液 混合溶液 | 开始时阴极无红色物质析出 | 氧化性: |
| A.A | B.B | C.C | D.D |
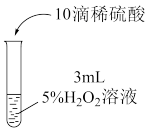
| 序号 | ① | ② | ③ |
| 实验装置及操作 |
|
|
|
| 实验现象 | 溶液无明显变化 | 溶液立即变为黄色,产生大量无色气体;溶液温度升高;最终溶液仍为黄色 | 溶液立即变为棕黄色,产生少量无色气体;溶液颜色逐渐加深,温度无明显变化;最终有紫黑色沉淀析出 |
A. 对 对 分解有催化作用 分解有催化作用 |
B.对比②和③,酸性条件下 氧化 氧化 的速率更大 的速率更大 |
C.对比②和③,②中的现象可能是因为 分解的速率大于H2O2氧化 分解的速率大于H2O2氧化 的速率 的速率 |
D.实验②③中的温度差异说明, 氧化 氧化 的反应放热 的反应放热 |
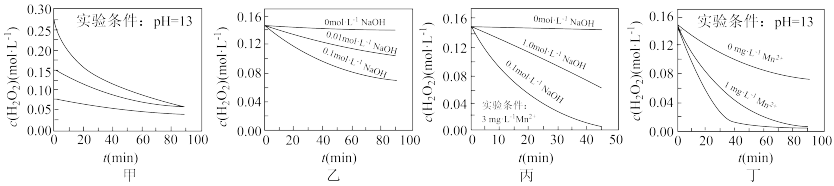
| A.图甲表明,其他条件相同时,H2O2浓度越大,其分解速率越快 |
| B.图乙表明,其他条件相同时,NaOH溶液浓度越小,H2O2分解速率越慢 |
| C.图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快 |
| D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大 |