氢键与沸点的关系(结构决定性质)
偶然的机会,碰到个问题,正丁醇的沸点大于异丁醇,又大于叔丁醇。同样都是醇类物质,原子个数一样,排列不一样,我们称之为同分异构体。常识告诉我们,沸点就是分子克服液相时候的分子间作用力,跑到气相的过程,还涉及到饱和蒸气压(这个这次我们就不讨论)。分子间的作用力主要有氢键和范德华作用力。氢键的作用力介乎于分子内(化学键)作用力和分子间之间,数量级上一般比范德华作用力大1-2数量级(10-100)。因此,我们这次考虑的是三种同分异构体的分子间氢键的差异。
氢键形成的条件:1.H-X,极性的键,X的强电负性导致氢原子的原子核接近裸露;2.孤对电子(O,N,S,F等元素)与氢原子共用电子对,从而形成氢键。
通过量化计算(Gaussian09软件)发现,由于甲基的供电子效应,羟基氧上的负电荷呈减少加趋势,正、异、叔化合物的羟基氧的电荷分别是-0.616,-0.593,-0.583。
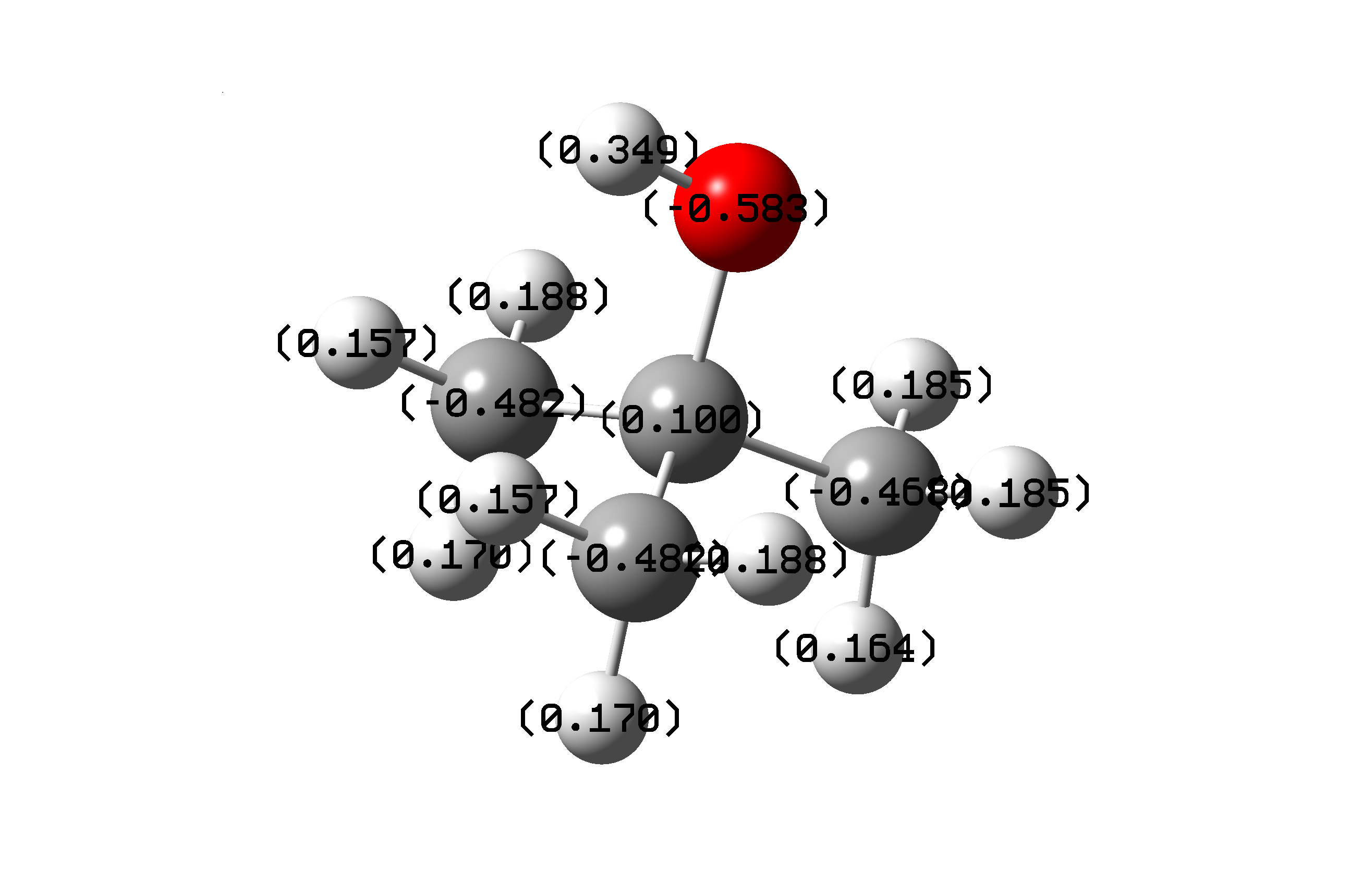
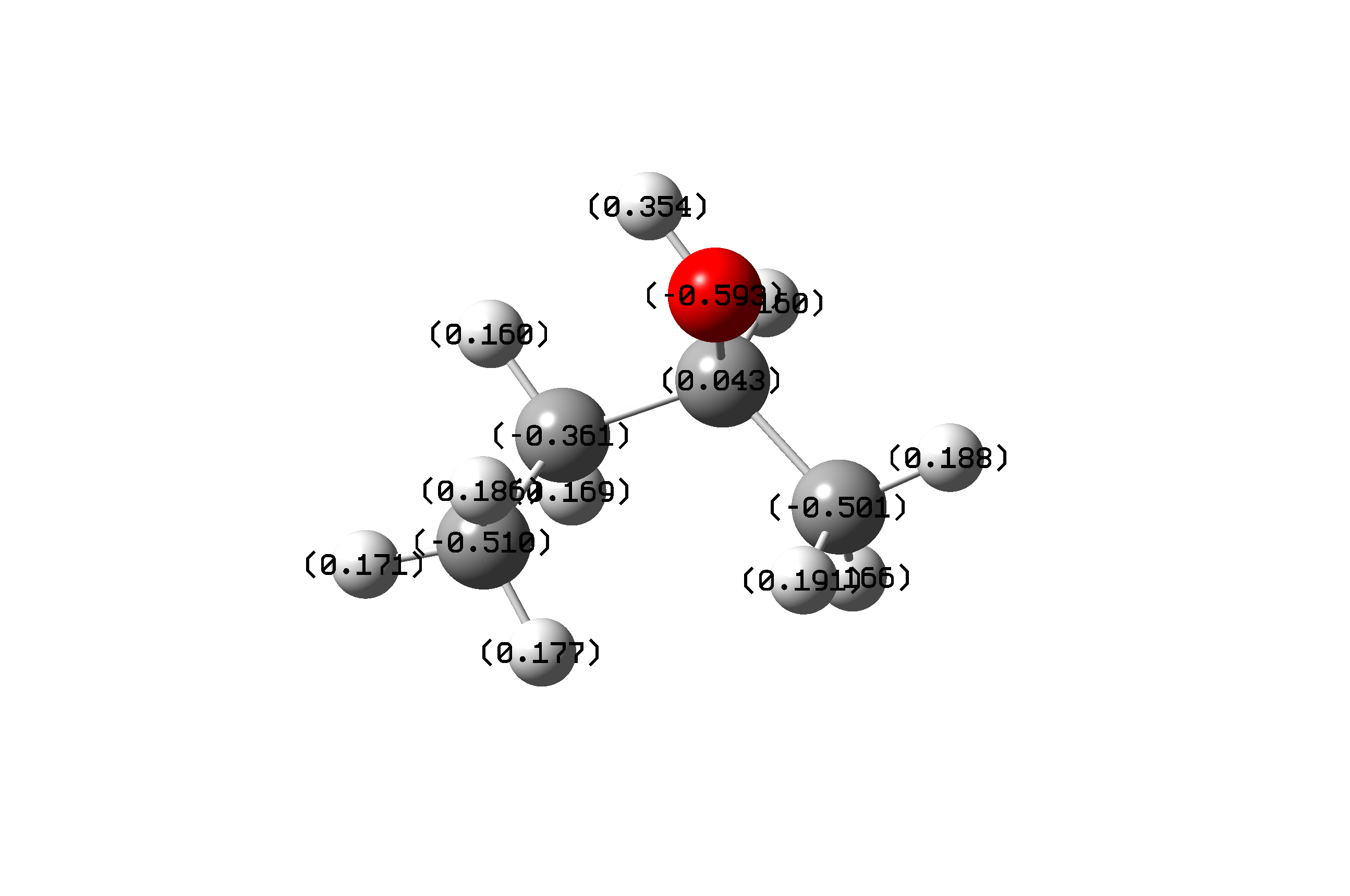
图1 异丁醇和叔丁醇的电荷分布示意图
结合氢键形成的条件,我们可以判断,供电子基团导致氧原子上的电子增多,羟基的O-H键极性变弱,分子间氢键作用变弱。
文章被以下专栏收录


