2020—2021 学年下学期高一期中考试化学试题
2020—2021 学年下学期高一期中考试化学试题
注意事项:
1.答题前,考生务必将自己的姓名、准考证条形码贴在答题卡指定位置。
2.选择题的作答:每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。 写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题作答:用黑色签字笔直接答在答题卡上对应的答题区域内,写在试题卷、 草稿纸和答题卡上的非答题区域均无效。
4.考生务必保持答题卡的整洁,考试结束后请将答题卡上交。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Zn 65 Cu 64
一、选择题(本题共 15 小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一 项是符合题目要求的。)
1.3 月 15 日,我国遭遇近十年最强沙尘天气,受此次沙尘天气影响,襄阳的空气质量也受 到了严重的污染,下列关于环境的叙述中正确的是
A.正常雨水的 pH 为 5.6,主要是因为溶解了 SO2
B.利用太阳能、风能和氢能替代化石能源可以改善空气的质量
C.为防止生活中使用过的废旧电池污染环境,应将废电池埋入土里
D.燃煤中加入生石灰既可减少酸雨的产生,又可减少温室气体的排放
2.NA 为阿伏加德罗常数,下列叙述正确的是
A.常温常压下,2.24 L NH3 中含有的原子数为 0.4NA B.1 mol Cu 与过量的稀 HNO3 反应,转移 2NA 个电子
C.密闭容器中,2 mol SO2 和 1 mol O2 催化反应后分子总数为 2NA
D.常温常压下,1.8 g D2O 中所含原子数为 0.3NA
3.下列说法正确的是
A.NH3 易液化,液氨常用作制冷剂
B.高纯度的硅单质可用于制作光导纤维
C.水晶、石英、玻璃、水泥都是常见的硅酸盐材料 D.在玻璃熔窑中制造普通玻璃不涉及化学变化
4.依据下图中氮元素及其化合物的转化关系,判断下列
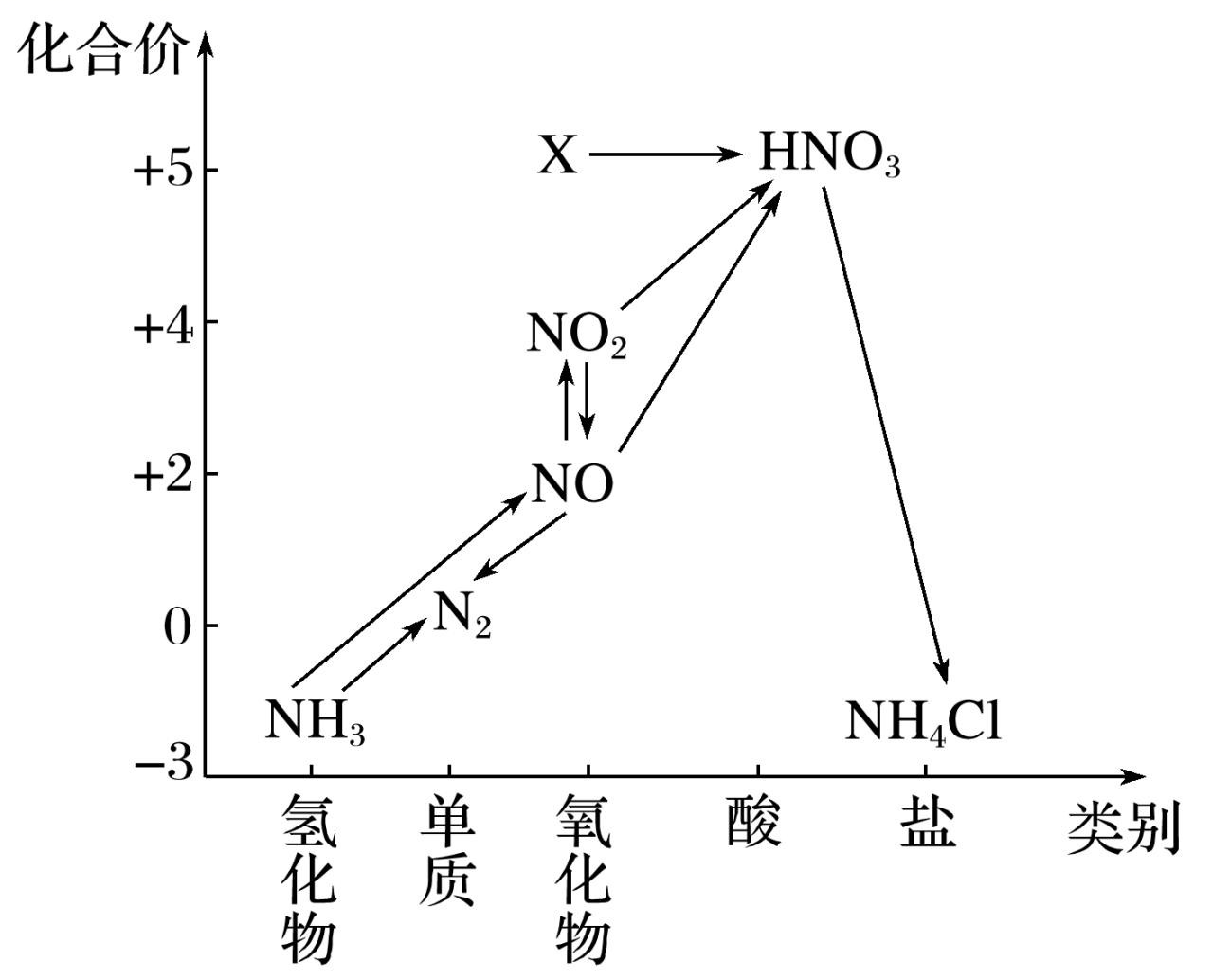
说法中不正确的是
A.X 是 N2O5
B.可用排水法收集 NO2 气体
C.工业上以 NH3、空气、水为原料生产硝酸
D.从原理上看,NH3 可与 NO2 反应实现 NH3→N2
的转化
5.把 X、Y、Z、W 4 种金属两两相连浸入稀硫酸中都可以组成原电池。若 X、Y 相连,X 为负极;Z、W 相连,W 上有气泡逸出;X、Z 相连时,X 质量减少;Y、W 相连,Y 为 正极。则四种金属的活动性顺序由大到小排列为
A.X > Z > Y > W B.Y > W > Z > X C.X > Z > W > Y D.X > Y > Z > W
6.下列由实验操作及现象得出的结论正确的是
A.向某溶液中加入 AgNO3 溶液,有白色沉淀生成,说明原溶液中一定含有 Cl-
B.向某溶液中加入浓的 NaOH 溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝, 说明原溶液中存在 NH4+
C.过量铜与稀硝酸充分反应后再滴加稀硫酸,铜逐渐溶解,说明铜可以和稀硫酸反应
D.常温下,将铁片放入浓硫酸中,无明显现象,说明铁不与冷的浓硫酸反应
7.下列说法不正确的是
A.增大压强,化学反应速率可能加快
B.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
C.需要加热才能发生的反应一定是吸热反应
D.“煮豆燃豆萁,豆在釜中泣”,句中涉及的能量变化主要是化学能转化为热能和光能
8.在 2A(g) + 3B(g) == 2C(g) + D(s)反应中,表示反应速率最快的是
A.v(A)=0.5 mol·L-1·min-1 B.v(B)=0.6 mol·L-1·min-1
C.v(C)=0.45 mol·L-1·min-1 D.v(D)=0.2 mol·L-1·min-1
9.一定温度下在一定体积的密闭容器中,下列叙述能作为可逆反应 N2(g) + 3H2(g) ⇌ 2NH3(g)
达到平衡状态标志的是
①NH3 的生成速率与 NH3 的消耗速率相等
②单位时间内断裂 3 mol H—H 键,同时断裂 2 mol N—H 键
③混合气体的总压强不再变化
④混合气体的平均相对分子质量不再变化
⑤混合气体的密度保持不变
⑥N2、H2 和 NH3 的分子数之比为 1∶3∶2
A.①③④ B.①④⑤ C.③④⑥ D.②⑤⑥
10.化学反应常常伴随能量的变化,以下是 H2 与 Cl2 反应的能量变化示意图,下列说法正确 的是

A.氯化氢分子的电子式:
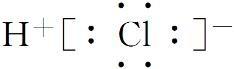
B.形成 1 mol H—Cl 键要吸收 431 kJ 的能量
C.该反应既是氧化还原反应又是放热反应
D.反应物断键时吸收的能量大于产物形成化学键时释放的能量
11.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧
化 钾 溶 液 为 电 解 液 , 电 池 总 反 应 式 为 Zn(s) + 2MnO2(s) + H2O(l) == Zn(OH)2(s) + Mn2O3(s),下列说法错误的是
A.电池工作时,锌失去电子
B.电池工作时,电子由正极通过外电路流向负极 C.电池负极上发生氧化反应
D.外电路中每通过 0.4 mol 电子,锌的质量理论上减小 13.0 g
12.下列关于褪色原理叙述正确的是
A.SO2 可使溴水褪色,体现了 SO2 的漂白性
B.Cl2 可使湿润的有色布条褪色,说明 Cl2 具有漂白性
C.活性炭可以吸附有色物质,是因为活性炭可以与有色物质发生化合反应
D.向酸性 KMnO4 溶液中通入足量 SO2 气体,KMnO4 溶液褪色,说明 SO2 具有还原性
13.利用下列装置(部分仪器已省略),能顺利完成对应实验的是
A.排空气法收集氨气 B.构成原电池
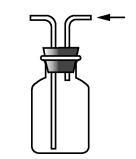
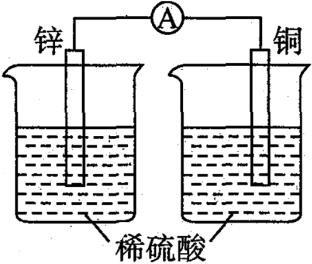
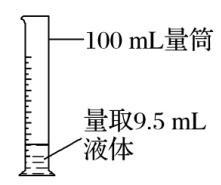
C.量取 9.5 mL 稀盐酸 D.喷泉实验

14.近日,国外服装企业 H&M 集团发布声明抵制新疆棉花产品,引起众怒。目前国内多个 电商平台已下架 H&M 相关产品。不仅是生活中,在化学实验中,我们也常常使用到棉 花。下列实验中,关于棉花团的用途叙述不正确的是

图一 图二
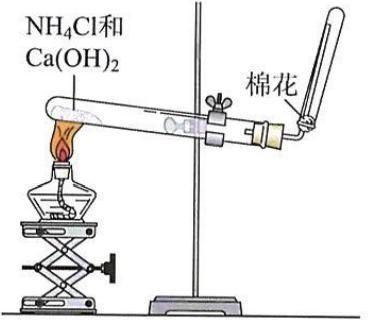
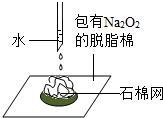
图三 图四
A.图一加热高锰酸钾固体制备氧气时,是为了防止高锰酸钾固体堵塞导气管 B.图二制取氨气时,干棉花是为了防止氨气逸出污染环境
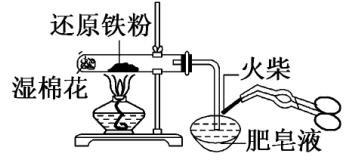
C.图三 Fe 与水蒸气反应时,是为了受热时提供高温水蒸气与铁粉反应
D.图四向包有 Na2O2 的脱脂棉上滴加几滴水,脱脂棉燃烧,说明 Na2O2 与水的反应是 放热反应
15.在一定温度条件下,将 1 mol A 和 2 mol B 放入容积为 5 L 的密闭容器中发生如下反应: A(s) + 2B(g) ⇌ C(g) + 2D(g),反应经 5 min 后达到平衡状态,测得容器内 B 物质的浓度 减少了 0.2 mol·L-1。下列叙述不正确的是
A.在 5 min 内该反应用 C 的浓度变化表示的反应速率 0.02 mol•L-1•min-1
B.平衡时 A、B 的转化率均为 50% C.初始压强和平衡时压强比为 4 : 5
D.平衡时混合气体中 B 的体积分数为 33.3%
二、填空题(本题共 4 小题,55 分)
16.(14 分)

工业上用 CO 生产燃料甲醇,一定条件下发生反应: CO(g) + 2H2(g) ⇌ CH3OH(g),反应过程中的能量变化情 况如图所示,曲线 Ⅰ 和曲线 Ⅱ 分别表示不使用催化剂和 使用催化剂的两种情况。
(1)观察图象可知上述反应过程中,断裂反应物中
的化学键吸收的总能量 (填“大于”、“小于”或“等于”)形成生成物中的化学 键释放的总能量。计算当反应生成 1.5 mol CH3OH(g)时,能量变化值是 kJ。
(2)根据上图分析,选择适宜的催化剂 (填“能”或“不能”)改变该反应
过程中的能量变化。
(3)推测反应 CH3OH(g) ⇌ CO(g)+2H2(g)是 (填“吸热”或“放热”)反应。
(4)燃料电池的工作原理是将燃料和氧化剂(O2 反应所产生的能量直接转化为电能。中国科学院长春 应用化学研究所在甲醇(CH3OH)燃料电池技术方面 获得新突破,甲醇燃料电池(DMFC)具备低温快速 启动、体积小巧、燃料使用便利、电池的比能量高的 特性,这使得甲醇燃料电池可能成为未来便携式电子 产品应用的主流。甲醇燃料电池的工作原理如右图所 示。
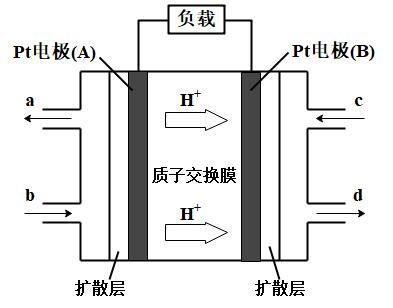
①Pt 电极(A)是燃料电池的 (填“正”或“负”)极,b 处通入的是 。
②该电池正极上的电极反应式为 。
17.(14 分) 根据化学反应速率与化学反应限度的知识回答下列问题。

(1)在 2 L 恒容的密闭容器内充入 0.30 mol 的 X
气体和 0.20 mol 的 Y 气体,在一定条件下反应生成气体
Z。反应体系中,各组分的物质的量随时间的变化如图
①该反应的化学方程式为 。
②反应进行到 5 s 时,是否达到平衡状态?
(填“是”或“否”),12 s 时,v 正(Z) v 逆(Z)(填 “大于”、“小于”或“等于”)。
③用 X 的浓度变化表示从 0 ~ 5 s 内该反应的平均速率 v(X) = 。
(2)已知合成氨反应的化学方程式为 N2(g) + 3H2(g) ⇌ 2NH3(g),该反应为放热反应, 且每生成 2 mol NH3,放出 92.4 kJ 的热量。在一定温度下,向一个容积为 1 L 的密闭容器中 通入 2 mol N2 和 8 mol H2 及固体催化剂,使之反应,达到平衡时容器内气体的压强为起始时 的 80%,则:
①平衡时 NH3 的物质的量为 ,H2 的转化率为 ;
②反应达到平衡时,放出的热量
A.小于 92.4 kJ B.等于 92.4 kJ
C.大于 92.4 kJ D.可能大于、小于或等于 92.4 kJ
18.(14 分)
某研究小组用如图装置进行 SO2 与 FeCl3 溶液反应的相关实验(夹持装置已略去)。

(1)A 中发生反应的化学方程式为 。
(2)通入足量 SO2 时 C 中观察到的现象为 。
(3)根据以上现象,该小组同学认为 SO2 与 FeCl3 溶液发生氧化还原反应。
①写出 SO2 与 FeCl3 溶液反应的离子方程式 。
②该小组同学向 C 试管反应后的溶液中加入硝酸酸化的 BaCl2 溶液,若出现白色沉淀,
2-
即可证明反应生成了 SO4
。该做法 (填“合理”或“不合理”),理由是
。
(4)D 装置中倒置漏斗的作用是 。
(5)为了验证 SO2 具有还原性,实验中可以代替 FeCl3 的试剂有 。
a.浓硫酸 b.酸性 KMnO4 溶液 c.碘水 d.NaCl 溶液
19. (13 分) 工业上硝酸的制备和自然界中硝酸的生成既有相同之处,又有区别。图中路线 a、b、c
是工业制备硝酸的主要途径,路线Ⅰ、Ⅱ、Ⅲ是雷电固氮过程中生成硝酸的途径。

(1)N2 在常温下性质很稳定,任意写出一种与此性质有关的用途: 。
(2)实验室制取 NH3 的化学方程式为 。
(3)NH3 的电子式为 。
(4)下列环境问题与氮的氧化物排放无关的是 ;
A. 酸雨 B. 光化学烟雾 C. 臭氧层空洞 D.白色污染
(5)Ertl(获 2007 年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于 汽车尾气处理中,在催化剂存在下可将 NO 和 CO 反应转化为两种无色无毒气体,用化学反 应方程式表示这个过程 ;氧化产物与还原产物的物质的量之比为 。
(6)64.0 g Cu 与适量的浓 HNO3 反应,铜全部溶解后,共收集到 1 mol NO2 和 NO 的混合气体,
反应中消耗 HNO3 的物质的量是 。
文章被以下专栏收录


