如何通俗易懂地解释 dsp² 杂化轨道为何呈平面四方形?
4 个回答
本来觉得是个很简单的问题翻个书就能答,后来发现还挺麻烦的。
通俗易懂的解释大约就是从对称性考虑:d(x2-y2), s, px, py这四个轨道都分布在x-y这个平面内,因此杂化之后的轨道也没有z轴方向的分量。
深究的话还是晶体场理论更好一些,再深一步直接从能量最低的角度模拟优化分子结构吧……
以前学竞赛的时候也纠结过这个,书上要么没有解释,要么直接说这是算出来的。这是我自己想出来的解释方法,个人认为比较通俗易懂直观(虽然不太严谨):
dsp² 杂化轨道是由 s px py dx²-y² 这四个原子轨道线性组合而来,通过结构化学轨道对称性的知识,可以算出(不会算也不影响理解)每个杂化轨道所含有的四个原子轨道的系数。

不会算并不影响理解,因为我们不必关注系数的值,只需要看每一项的正负号,然后把对应轨道画出来。
比如 ψ₁ 轨道是 s d px 三个组合而来,在 x 轴正方向每个轨道都是正号,其他方向则各有抵消,所以杂化轨道应该最大波瓣取向为 x 正半轴方向。

同理也可以分析出剩下三个轨道是沿着另外三个方向,整体就是沿着四个轴的平面四方分布。
另外,sp、sp²、sp³、d²sp³ 等简单杂化轨道都可以用这种方法画出最大波瓣的空间取向分布。
比如下图以sp³的第一个杂化轨道为例,三个 p 轨道在第一卦限(三个轴的正方向)均为正,第七卦限(三个轴的负方向)都为负,其他方向各自抵消。再加上整体为正的 s 轨道,所以杂化轨道最大波瓣是沿着 (1,1,1) 方向的。
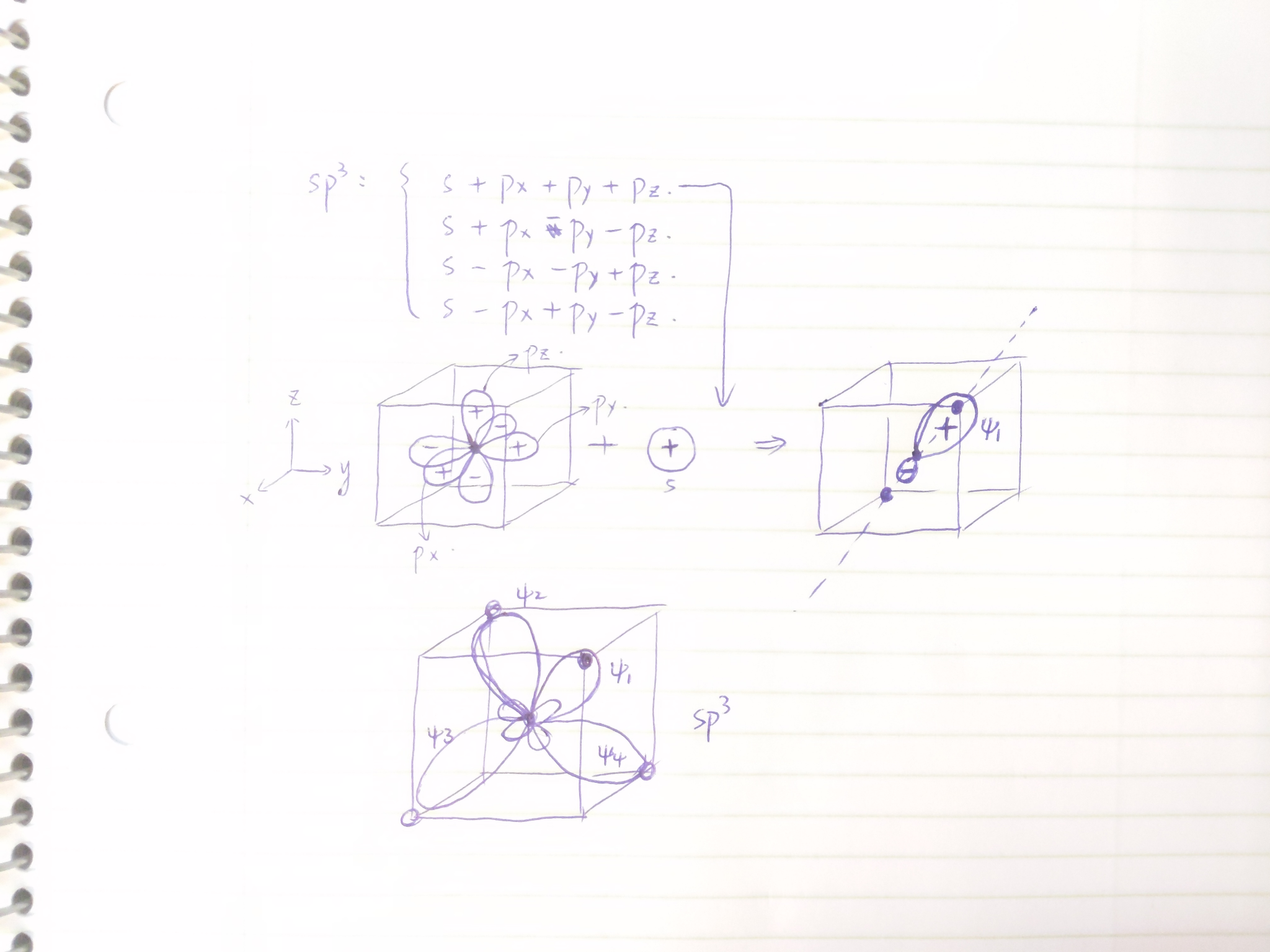
而四个都画出来则是最下面这样(画得有点丑),也就是 sp³ 的正四面体排布。
dsp2杂化中d和p用的轨道是 d_{x^2-y^2} 和 p_xp_y 这些轨道,它们的线性组合自然组成了一个平面正方形。
来一个不是特别通俗易懂的答案





