含氮杂环化合物及其中间体的合成方法与流程
1.本发明涉及有机合成技术领域,特别是涉及一种含氮杂环类化合物及其中间体的合成方法。
背景技术:
2.含氮杂环化合物在药物化学技术领域具有十分重要的研究地位。一方面,含氮杂环化合物易于进行结构修饰,便于引入各种官能团,因此在过去的几十年中,含氮杂环化合物在药物设计中发挥了重要作用。另一方面,很多药物先导分子都含有含氮杂环化合物结构,且部分含氮杂环化合物被发现其本身即具有一定的生物活性,如抗癌、抗氧化、抗菌、抗病毒、抗真菌、抗炎等,可以作为生物活性分子的重要合成砌块。
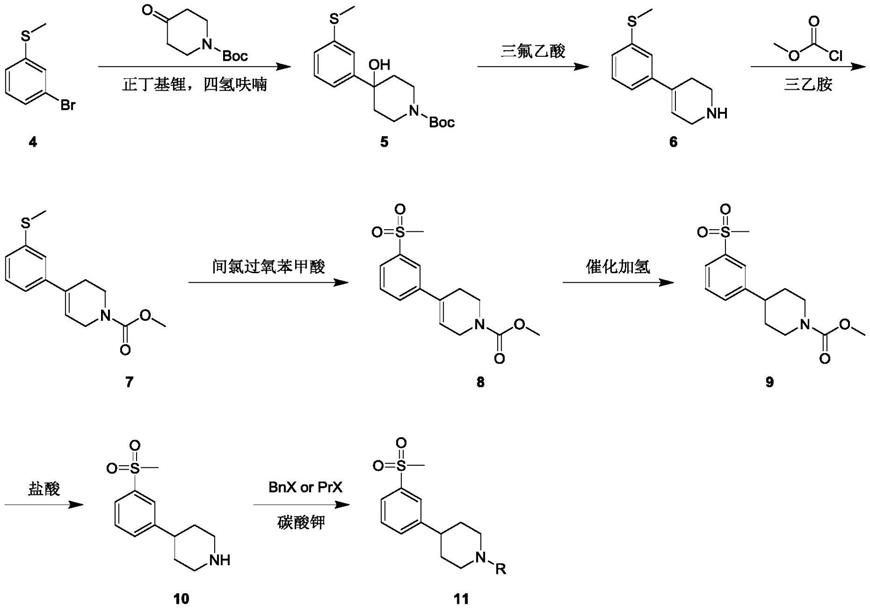
3.有文献涉及了一系列4-苯基哌啶和4-苯基哌嗪做为d2受体配体的合成与评价及多巴胺能稳定剂4-[3-(甲基磺酰基)苯基]-1-丙基哌啶(huntexil,pridopidine,acr16)的发现。其中,涉及到化合物11的合成路线如下所示:
[0004][0005]
化合物4与n-叔丁氧羰基-4-哌啶酮在正丁基锂作用下,生成化合物5;化合物5在三氟乙酸作用下脱保护脱水得到化合物6;化合物6在三乙胺作用下与氯甲酸甲酯反应得到化合物7;化合物7经间氯过氧苯甲酸氧化得到化合物8;化合物8催化加氢得到化合物9;化合物9盐酸脱乙酰基得到化合物10;化合物10与卤代物在碳酸钾的作用下反应得到化合物11(4-[3-(甲基磺酰基)苯基]-1-丙基哌啶或者4-[3-(甲基磺酰基)苯基]-1-苄基哌啶)。
[0006]
该合成方法路线冗长,且使用了国家监管剧毒品(氯甲酸甲酯),同时还需要采用
催化加氢等存在安全隐患的反应,原料与设备成本高,不利于工业放大生产。
技术实现要素:
[0007]
基于此,本发明提供一种路线短、操作安全、成本低,便于工业化放大生产的含氮杂环化合物及其中间体的合成方法。
[0008]
本发明的第一方面,提供一种含氮杂环类化合物的中间体合成方法,包括如下步骤:
[0009]
将化合物1和化合物2进行光化学反应,制备所述中间体;
[0010]
所述化合物1的结构如下所示:
[0011][0012]
所述化合物2的结构如下所示:
[0013][0014]
所述中间体的结构如下所示:
[0015][0016]
其中,y1、y2、y3、y4、y5各自独立地为ch2或nr,且至少一个为nr;r表示保护基;
[0017]
x1、x2各自独立地为卤素;
[0018]
ar为c6~c10芳基或c5~c10杂芳基;
[0019]
r1、r2各自独立地为氢、卤素、氰基、羟基、c1~c6烷氧基或-s(o)2r3,r3为c1~c6烷基。
[0020]
在其中一个实施例中,光化学反应采用的光源为8w~12w的蓝光灯。
[0021]
在其中一个实施例中,光化学反应的条件包括:在溶剂、有机铱配合物光催化剂、镍试剂、硅试剂和碱存在的条件下进行反应。
[0022]
在其中一个实施例中,所述溶剂选自乙二醇二甲醚、乙腈、n,n-二甲基乙酰胺和n,n-二甲基甲酰胺中的一种或多种;及/或所述碱选自碳酸钠、碳酸钾和氢氧化锂中的一种或多种;及/或
[0023]
所述硅试剂选自三乙基硅烷、三(三甲基硅基)硅烷和三苯基硅烷中的一种或多种;及/或
[0024]
所述有机铱配合物光催化剂选自三(2-苯基吡啶)合铱和[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)中的一种或两种;及/或
[0025]
所述镍试剂为[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)。
[0026]
在其中一个实施例中,光化学反应的条件包括:于20℃~30℃条件下反应10h~20h。
[0027]
在其中一个实施例中,y1、y2、y3、y4、y5选自如下组之一:
[0028]
(i)y1为nr,y2、y3、y4和y5为ch2;
[0029]
(ii)y2为nr,y1、y3、y4和y5为ch2;
[0030]
(iii)y4为nr,y1、y2、y3和y5为ch2;
[0031]
(iv)y1和y3为nr,y4、y2和y5为ch2。
[0032]
在其中一个实施例中,x1、x2为-br。
[0033]
在其中一个实施例中,ar具有如下所示结构特征:
[0034][0035]
其中,y6各自独立地选自ch或n。
[0036]
在其中一个实施例中,r1、r2各自独立地为羟基或c1~c3烷氧基。
[0037]
本发明的第二方面,提供一种含氮杂环类化合物的合成方法,包括如下步骤:
[0038]
按照第一方面所述的合成方法制备所述中间体;
[0039]
对所述中间体进行脱保护反应,制备所述含氮杂环类化合物;
[0040]
所述含氮杂环类化合物的结构如下所示:
[0041][0042]
其中,ar、r1和r2的定义同权利要求1;
[0043]
w1、w2、w3、w4、w5各自独立地为ch2或nh,且至少一个为nh。
[0044]
在其中一个实施例中,脱保护反应在酸存在的条件下进行。
[0045]
上述合成方法通过以特定结构的化合物1和化合物2作为起始原料,结合光化学反应,实现了含氮杂环类化合物及其中间体的合成。同时,该合成方法的路线短,且反应条件温和,无需加压或采用管制试剂,操作安全、简便,起始原料便宜易得,便于工业化放大生产。
具体实施方式
[0046]
以下结合具体实施例对本发明的含氮杂环类化合物及其中间体的合成方法作进一步详细的说明。本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式。相反地,提供这些实施方式的目的是使对本发明公开内容理解更加透彻全面。
[0047]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
[0048]
本发明中,“第一方面”、“第二方面”等仅用于描述目的,不能理解为指示或暗示相
对重要性或数量,也不能理解为隐含指明所指示的技术特征的重要性或数量。而且“第一”、“第二”等仅起到非穷举式的列举描述目的,应当理解并不构成对数量的封闭式限定。
[0049]
本发明中,以开放式描述的技术特征中,包括所列举特征组成的封闭式技术方案,也包括包含所列举特征的开放式技术方案。
[0050]
本发明中,涉及到数值区间,如无特别说明,上述数值区间内视为连续,且包括该范围的最小值及最大值,以及这种最小值与最大值之间的每一个值。进一步地,当范围是指整数时,包括该范围的最小值与最大值之间的每一个整数。此外,当提供多个范围描述特征或特性时,可以合并该范围。换言之,除非另有指明,否则本文中所公开之所有范围应理解为包括其中所归入的任何及所有的子范围。
[0051]
本发明中,涉及的百分比含量,如无特别说明,对于固液混合和固相-固相混合均指质量百分比,对于液相-液相混合指体积百分比。
[0052]
本发明中,涉及的百分比浓度,如无特别说明,均指终浓度。所述终浓度,指添加成分在添加该成分后的体系中的占比。
[0053]
本发明中,如无特别限定,温度参数既允许为恒温处理,也允许在一定温度区间内进行处理。所述的恒温处理允许温度在仪器控制的精度范围内进行波动。
[0054]
本发明中,“卤素”是指f、cl、br或i。
[0055]
本发明中,“芳基”是指在芳香环化合物的基础上除去一个氢原子衍生的芳族烃基,可以为单环芳基、或稠环芳基、或多环芳基,对于多环的环种,至少一个是芳族环系。例如,“c6~c10芳基”是指包含6至10个碳原子的芳基,每次出现时,可以互相独立地为c6芳基、c7芳基、c8芳基、c9芳基或c10芳基。合适的实例包括但不限于:苯、联苯、萘、蒽、菲、二萘嵌苯、三亚苯及其衍生物。
[0056]
本发明中,“杂芳基”是指在芳基的基础上至少一个碳原子被非碳原子所替代,非碳原子可以为n原子、o原子、s原子等。例如,“c5~c10杂芳基”是指包含5至10个碳原子的杂芳基,每次出现时,可以互相独立地为c5杂芳基、c6杂芳基、c7杂芳基、c8杂芳基、c9杂芳基或c10杂芳基。合适的实例包括但不限于:呋喃、苯并呋喃、噻吩、苯并噻吩、吡咯、吡唑、三唑、咪唑、噁唑、噁二唑、噻唑、四唑、吲哚、咔唑、吡咯并咪唑、吡咯并吡咯、噻吩并吡咯、噻吩并噻吩、呋喃并吡咯、呋喃并呋喃、噻吩并呋喃、苯并异噁唑、苯并异噻唑、苯并咪唑、吡啶、吡嗪、哒嗪、嘧啶、三嗪、喹啉、异喹啉、邻二氮萘、喹喔啉、菲啶、伯啶、喹唑啉和喹唑啉酮。
[0057]
本发明中,术语“烷基”是指包含伯(正)碳原子、或仲碳原子、或叔碳原子、或季碳原子、或其组合的饱和烃失去一个氢原子生成的一价残基。包含该术语的短语,例如,“c1~c6烷基”是指包含1~6个碳原子的烷基,每次出现时,可以互相独立地为c1烷基、c2烷基、c3烷基、c4烷基、c5烷基或c6烷基。合适的实例包括但不限于:甲基(me、-ch3)、乙基(et、-ch2ch3)、1-丙基(n-pr、n-丙基、-ch2ch2ch3)、2-丙基(i-pr、i-丙基、-ch(ch3)2)、1-丁基(n-bu、n-丁基、-ch2ch2ch2ch3)、2-甲基-1-丙基(i-bu、i-丁基、-ch2ch(ch3)2)、2-丁基(s-bu、s-丁基、-ch(ch3)ch2ch3)、2-甲基-2-丙基(t-bu、t-丁基、-c(ch3)3)、1-戊基(n-戊基、-ch2ch2ch2ch2ch3)、2-戊基(-ch(ch3)ch2ch2ch3)、3-戊基(-ch(ch2ch3)2)、2-甲基-2-丁基(-c(ch3)2ch2ch3)、3-甲基-2-丁基(-ch(ch3)ch(ch3)2)、3-甲基-1-丁基(-ch2ch2ch(ch3)2)、2-甲基-1-丁基(-ch2ch(ch3)ch2ch3)、1-己基(-ch2ch2ch2ch2ch2ch3)、2-己基(-ch(ch3)ch2ch2ch2ch3)、3-己基(-ch(ch2ch3)(ch2ch2ch3))、2-甲基-2-戊基(-c(ch3)2ch2ch2ch3)、3-甲
基-2-戊基(-ch(ch3)ch(ch3)ch2ch3)、4-甲基-2-戊基(-ch(ch3)ch2ch(ch3)2)、3-甲基-3-戊基(-c(ch3)(ch2ch3)2)、2-甲基-3-戊基(-ch(ch2ch3)ch(ch3)2)、2,3-二甲基-2-丁基(-c(ch3)2ch(ch3)2)、3,3-二甲基-2-丁基(-ch(ch3)c(ch3)3)。
[0058]
本发明中,“烷氧基”是指结构为-o-烷基的基团,即如上所定义的烷基经由氧原子连接至相邻基团。包含该术语的短语,例如,“c1~c6烷氧基”是指烷基部分包含1~6个碳原子,每次出现时,可以互相独立地为c1烷氧基、c2烷氧基、c3烷氧基、c4烷氧基、c5烷氧基、c6烷氧基。合适的实例包括但不限于:甲氧基(-o-ch3或-ome)、乙氧基(-o-ch2ch3或-oet)和叔丁氧基(-o-c(ch3)3或-otbu)。
[0059]
本发明中,“*”表示连接位点。
[0060]
本发明的提供一种含氮杂环类化合物的中间体合成方法,包括如下步骤:
[0061]
将化合物1和化合物2进行光化学反应,制备所述中间体;
[0062]
所述化合物1的结构如下所示:
[0063][0064]
所述化合物2的结构如下所示:
[0065][0066]
所述中间体的结构如下所示:
[0067][0068]
其中,y1、y2、y3、y4、y5各自独立地为ch2或nr,且至少一个为nr;r表示保护基;
[0069]
x1、x2各自独立地为卤素;
[0070]
ar为c6~c10芳基或c5~c10杂芳基;
[0071]
r1、r2各自独立地为氢、卤素、氰基、羟基、c1~c6烷氧基或-s(o)2r3,r3为c1~c6烷基。
[0072]
在其中一个具体的示例中,光化学反应采用的光源为8w~12w的蓝光灯。具体地,光化学反应采用的光源的功率包括但不限于:8w、9w、10w、11w、12w。可以理解地,蓝光灯是指发射蓝光的灯源,蓝光是指波长为480~500nm的光线。具体地,蓝光灯可为蓝色led灯。
[0073]
在其中一个具体的示例中,蓝光灯与反应物之间的距离为2cm~5cm。
[0074]
在其中一个具体的示例中,光化学反应的条件包括:在溶剂、有机铱配合物光催化剂、镍试剂、硅试剂和碱存在的条件下进行反应。
[0075]
具体地,溶剂选自乙二醇二甲醚、乙腈、n,n-二甲基乙酰胺和n,n-二甲基甲酰胺中的一种或多种。进一步地,溶剂为乙二醇二甲醚。
[0076]
具体地,碱选自碳酸钠、碳酸钾和氢氧化锂中的一种或多种。进一步地,碱为碳酸钠。
[0077]
具体地,硅试剂选自三乙基硅烷、三(三甲基硅基)硅烷和三苯基硅烷中的一种或多种。进一步地,硅试剂为三(三甲基硅基)硅烷。
[0078]
具体地,有机铱配合物光催化剂选自三(2-苯基吡啶)合铱和[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)(cas:870987-63-6)中的一种或两种。进一步地,有机铱配合物光催化剂为[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)。
[0079]
具体地,镍试剂为[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)。
[0080]
在其中一个具体的示例中,光化学反应的条件包括:以乙二醇二甲醚为溶剂,在[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)、[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)、三(三甲基硅基)硅烷和碱存在的条件下进行反应。
[0081]
在其中一个具体的示例中,化合物2与化合物1的摩尔比为1:(1~1.5)。
[0082]
在其中一个具体的示例中,化合物2、[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)、[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)与三(三甲基硅基)硅烷的摩尔比为1:(0.005~0.015):(0.01~0.02):(0.8~1.2)。
[0083]
在其中一个具体的示例中,化合物2与碱的摩尔比为1:(1.5~3)。
[0084]
在其中一个具体的示例中,乙二醇二甲醚的用量为每1mmol的化合物2加入5ml~15ml。
[0085]
在其中一个具体的示例中,光化学反应的条件包括:于20℃~30℃条件下反应10h~20h。具体地,光化学反应的温度包括但不限于:20℃、21℃、22℃、23℃、24℃、25℃、26℃、27℃、28℃、29℃、30℃。具体地,光化学反应的时间包括但不限于:10h、11h、12h、13h、14h、15h、16h、17h、18h、19h、20h。
[0086]
另外,关于化合物1的结构:
[0087]
可以理解地,r表示保护基,可选用本领域现有的氨基保护基。在其中一个具体的示例中,r为叔丁氧羰基(-boc)。
[0088]
在其中一个具体的示例中,y1、y2、y3、y4、y5选自如下组之一:
[0089]
(i)y1为nr,y2、y3、y4和y5为ch2;
[0090]
(ii)y2为nr,y1、y3、y4和y5为ch2;
[0091]
(iii)y4为nr,y1、y2、y3和y5为ch2;
[0092]
(iv)y1和y3为nr,y4、y2和y5为ch2。
[0093]
进一步地,具有如下所示结构特征:
[0094]
在其中一个具体的示例中,化合物1选自如下化合物:
[0095][0096]
进一步地,关于化合物2的结构:
[0097]
可以理解地,r1、r2与x2连接至ar的位置不作限定,可以为临位、间位或对位。
[0098]
在其中一个具体的示例中,x1、x2各自独立地为-cl、-br或-i。进一步地,x1、x2为-br。
[0099]
在其中一个具体的示例中,ar具有如下所示结构特征:
[0100][0101]
其中,y6各自独立地选自ch或n。
[0102]
在其中一个具体的示例中,ar为苯基或吡啶基。进一步地,ar为苯基。
[0103]
在其中一个具体的示例中,r1、r2各自独立地为氢、-cl、羟基、c1~c3烷氧基或-s(o)2r3,r3为c1~c2烷基。进一步地,r1为氢,r2为-cl、羟基、c1~c3烷氧基或-s(o)2r3,r3为c1~c2烷基。
[0104]
在其中一个具体的示例中,r1、r2各自独立地为羟基或c1~c3烷氧基。
[0105]
在其中一个具体的示例中,化合物2选自如下化合物:
[0106][0107]
在其中一个具体的示例中,中间体选自如下化合物:
[0108][0109]
本发明提供一种含氮杂环类化合物的合成方法,包括如下步骤:
[0110]
按照如上述的合成方法制备所述中间体
1.57(m,2h),1.48(s,9h)。
[0124]
lc-ms:(m-55)
+
:240.0。
[0125]
hplc:99.5%purity(220nm,rt=3.081min)。
[0126]
实施例二 化合物a1的合成
[0127][0128]
化合物3a(20.0mg,67.6μmol,1.00eq)和盐酸/乙酸乙酯(4m,1ml)的混合物在15℃下搅拌反应2个小时。lcms监测反应结束后,反应液浓缩得到白色固体的化合物a1(15mg,64.3μmol,99.5%purity,95.1%yield)。
[0129]1h nmr:(400mhz,dmso-d6)δ9.08(br s,1h),7.41(d,j=8.4hz,2h),7.32(d,j=8.4hz,2h),,3.30-3.25(m,3h),3.03-2.98(m,2h),2.89-2.83(m,1h),1.88-1.65(m,4h)。
[0130]
lc-ms:(m+h)
+
:196.2。
[0131]
hplc:99.5%purity(220nm,rt=2.306min)。
[0132]
实施例三 化合物3b的合成
[0133][0134]
在氮气保护下,3-溴哌啶-1-甲酸叔丁酯(化合物1a)(68.4mg,0.260mmol,1.30eq),4-溴氯苯(化合物2b)(34.4mg,0.200mmol,1.00eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)(2.24mg,0.01eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)(1.19mg,0.015eq),三(三甲基硅基)硅烷(49.7mg,1.00eq),碳酸钠(42.4mg,2.00eq)和2毫升的乙二醇二甲醚加入到15毫升的反应瓶中,距离反应瓶3厘米的距离用10w的蓝色led灯照射,混合物25℃搅拌反应14个小时。lcms监测反应结束后,混合物过滤,滤液浓缩得到粗品。粗品用制备hplc分离得到白色固体的化合物3b(25mg,97.3%purity,45.1%yield)。
[0135]
h nmr:(400mhz,cdcl3)δ9.21(s,1h),7.03(d,j=8.4hz,2h),6.68(d,j=8.4hz,2h),3.96-3.88(m,2h),2.66-2.52(m,3h),1.82(d,j=12.4hz,1h),1.70-1.65(m,1h),1.59-1.50(m,1h),1.46-1.43(m,1h),1.39(s,9h)。
[0136]
lc-ms:(m-55)
+
:222.0。
[0137]
hplc:97.3%purity(220nm,rt=1.815min)。
[0138]
实施例四 化合物a2的合成
[0139][0140]
化合物3b(20.0mg,72.1μmol,1.00eq)和盐酸/乙酸乙酯(4m,1ml)的混合物在15℃下搅拌反应2个小时。lcms监测反应结束后,反应液浓缩得到白色固体的化合物a2(15mg,69.0μmol,98.3%purity,95.7%yield)。
[0141]1h nmr:(400mhz,dmso-d6)δ9.37(s,1h),9.03(br s,1h),7.05(d,j=8.4hz,2h),7.72(d,j=8.4hz,2h),3.26-3.18(m,2h),2.92-2.81(m,3h),1.86-1.57(m,4h)。
[0142]
lc-ms:(m+h)
+
:178.2。
[0143]
hplc:98.3%purity(220nm,rt=1.162min)。
[0144]
实施例五 化合物3c的合成
[0145][0146]
在氮气保护下,3-溴哌啶-1-甲酸叔丁酯(化合物1a)(68.4mg,0.260mmol,1.30eq),4-溴氯苯(化合物2c)(38.0mg,0.200mmol,1.00eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)(2.24mg,0.01eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)(1.19mg,0.015eq),三(三甲基硅基)硅烷(49.7mg,1.00eq),碳酸钠(42.4mg,2.00eq)和2毫升的乙二醇二甲醚加入到15毫升的反应瓶中,距离反应瓶3厘米的距离用10w的蓝色led灯照射,混合物25℃搅拌反应14个小时。lcms监测反应结束后,混合物过滤,滤液浓缩得到粗品。粗品用制备hplc分离得到白色固体的化合物3c(22mg,98.8%purity,37.3%yield)。
[0147]1h nmr:(400mhz,cdcl3)δ7.25-7.20(m,3h),7.10(d,j=7.2hz,1h),4.18-4.11(m,2h),2.78-2.65(m,3h),2.03-2.00(m,1h),1.78-1.74(m,1h),1.63-1.57(m,2h),1.48(s,9h)。
[0148]
lc-ms:(m-55)
+
:240.0。
[0149]
hplc:98.8%purity(220nm,rt=3.015min)。
[0150]
实施例六 化合物a3的合成
[0151][0152]
化合物3c(20.0mg,67.6μmol,1.00eq)和盐酸/乙酸乙酯(4m,1ml)的混合物在15℃下搅拌反应2个小时。lcms监测反应结束后,反应液浓缩得到粉色油状物的化合物a3(15mg,69.0μmol,98.6%purity,95.7%yield)。
[0153]1h nmr:(400mhz,dmso-d6)δ8.87(br s,1h),7.40(s,1h),7.37(d,j=7.6hz,1h),7.34-7.32(m,1h),7.27-7.25(m,1h),3.29-3.09(m,3h),3.06(t,j=12.4hz,1h),2.97(t,j=11.2hz,1h),2.87(t,j=12.4hz,1h),1.88(d,j=11.6hz,2h),1.77-1.67(m,2h)。
[0154]
lc-ms:(m+h)
+
:196.1。
[0155]
hplc:98.6%purity(220nm,rt=2.223min)。
[0156]
实施例七 化合物3d的合成
[0157][0158]
在氮气保护下,3-溴哌啶-1-甲酸叔丁酯(化合物1a)(68.6mg,0.260mmol,1.30eq),4-溴苯甲砜(化合物2d)(47.0mg,0.200mmol,1.00eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)(2.24mg,0.01eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)(1.19mg,0.015eq),三(三甲基硅基)硅烷(49.7mg,1.00eq),碳酸钠(42.4mg,2.00eq)和2毫升的乙二醇二甲醚加入到15毫升的反应瓶中,距离反应瓶3厘米的距离用10w的蓝色led灯照射,混合物25℃搅拌反应14个小时。lcms监测反应结束后,混合物过滤,滤液浓缩得到粗品。粗品用制备hplc分离得到淡黄色油状物的化合物3d(10mg,24.3μmol,95.8%purity,12.1%yield)。
[0159]1h nmr:(400mhz,cdcl3)δ7.89(d,j=8.2hz,2h),7.44(d,j=8.4hz,2h),4.38-3.98(m,2h),3.06(s,3h),2.79(s,3h),2.04(d,j=12.0hz,1h),1.83-1.74(m,1h),1.72-1.61(m,2h),1.48(s,9h)。
[0160]
lc-ms:(m-55)
+
:284.0。
[0161]
hplc:95.8%purity(220nm,rt=3.051min)。
[0162]
实施例八 化合物a4的合成
[0163][0164]
化合物3d(8.00mg,19.4μmol,1.00eq)和盐酸/二氧六环(4m,2ml)的混合物在25℃下搅拌反应0.5个小时。lcms监测反应结束后,反应液浓缩得到白色固体的化合物a4(5mg,17.7μmol,97.88%purity,91.27%yield)。
[0165]1h nmr:(400mhz,dmso-d6)δ9.29-9.12(m,1h),9.06-8.85(m,1h),7.91(d,j=8.4hz,2h),7.59(d,j=8.4hz,2h),3.32-3.27(m,2h),3.21(s,3h),3.14-3.06(m,2h),2.96-2.83(m,1h),1.93-1.71(m,4h)。
[0166]
lc-ms:(m+1)
+
:240.1。
[0167]
hplc:97.8%purity(220nm,rt=0.856min)。
[0168]
实施例九 化合物3e的合成
[0169][0170]
在氮气保护下,3-溴哌啶-1-甲酸叔丁酯(化合物1a)(827mg,3.14mmol,1.30eq),对溴苯甲醚(化合物2e)(450mg,2.42mmol.1.00eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基n]苯基-c]六氟磷酸铱(iii)(27.2mg,0.01eq),[4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
联吡啶n1,n1]二氯化镍(ii)(14.4mg,0.015eq),三(三甲基硅基)硅烷(602mg,1.00eq),碳酸钠(513mg,2.00eq)和24毫升的乙二醇二甲醚加入到40毫升的反应瓶中,距离反应瓶3厘米的距离用10w的蓝色led灯照射,混合物25℃搅拌反应14个小时。lcms监测反应结束后,混合物过滤,滤液浓缩得到粗品。粗品用制备hplc分离得到白色固体的化合物3e(450mg,1.54mmol,100%purity,45.0%yield)。
[0171]1h nmr:(400mhz,cdcl3)δ7.16(d,j=8.8hz,2h),6.86(d,j=8.4hz,2h),4.15(br s,2h),3.80(s,3h),2.74-2.63(m,3h),2.01-1.98(m,1h),1.76-1.74(m,1h),1.61-1.56(m,
2h),1.47(s,9h)。
[0172]
lc-ms:(m-55)+:236.2。
[0173]
hplc:100%purity(220nm,rt=2.452min)。
[0174]
实施例十 化合物a5的合成
[0175][0176]
化合物3e(20.0mg,68.6μmol,1.00eq)和盐酸/乙酸乙酯(4m,1ml)的混合物在15℃下搅拌反应0.5个小时。lcms监测反应结束后,反应液浓缩得到黄色固体的化合物a5(15.0mg,65.0umol,98.7%purity,94.7%yield)。
[0177]1h nmr:(400mhz,dmso-d6)δ8.91(br s,1h),8.65(br s,1h),7.19(d,j=8.8hz,2h),6.90(d,j=8.8hz,2h),3.73(s,3h),3.26(t,j=10.8hz,2h),2.97-2.85(m,3h),1.85(t,j=13.2hz,2h),1.76-1.67(m,2h)。
[0178]
lc-ms:(m+h)+:192.2。
[0179]
hplc:98.7%purity(220nm,rt=1.064min)。
[0180]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0181]
以上所述实施例仅表达了本发明的几种实施方式,便于具体和详细地理解本发明的技术方案,但并不能因此而理解为对发明专利保护范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。应当理解,本领域技术人员在本发明提供的技术方案的基础上,通过合乎逻辑的分析、推理或者有限的试验得到的技术方案,均在本发明所附权利要求的保护范围内。因此,本发明专利的保护范围应以所附权利要求的内容为准,说明书可以用于解释权利要求的内容。
- 一种通过光交联短肽定向固定化...
- 乳酸杆菌益生菌CGMCCNo...
- 高效扩增人流感病毒的方法和试...
- 一种X,γ射线防护用POE压...
- UBE2S调控PTEN-AK...
- 一种提升红法夫酵母菌株产虾青...
- 一类酚氧-吡啶螯合二氟化硼受...
- 氧-甲基转移酶PgmB在催化...
- 一种阳离子型水溶性近红外二区...
- 一种用于检测水体有机污染物的...
- 还没有人留言评论。精彩留言会获得点赞!