精英家教网> 试卷> 山东省肥城市二中2016年高中化学
第二章《化学物质及其变化》综合检测题 新人教版必修1 > 题目详情
-
网址:http://www.1010jiajiao.com/paper/timu/1491830.html [举报]
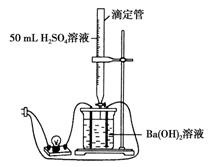
20.(8分)为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,实验设计和实验过程如下:
如图连接好装置,向烧杯中加入25 mL 1
mol/L的Ba(OH)2溶液和2滴酚酞试剂,再一边不断地滴加1 mol/L的H2SO4溶液,并轻轻振荡。试完成下列内容:
(1)实验现象及分析:①溶液颜色变化为_____________________________________,
原因___________________________________________________________________。
②灯泡亮度变化:_______________________________________________________,
原因___________________________________________________________________。
③溶液变浑浊,原因_____________________________________________________。
(2)实验结论:稀H2SO4与Ba(OH)2溶液反应的实质是_______________________ _________________________________________________(可用离子方程式解释)。
[答案] (1)①由红色逐渐变为浅红,最后颜色褪去 Ba(OH)2电离出的OH-与H2SO4电离出的H+中和生成H2O,使烧杯中的c(OH-)减小,红色逐渐褪去 ②随H2SO4溶液的不断加入,呈现出明到暗以至熄灭,再逐渐变亮 开始时,溶液中的离子浓度逐渐变小,故灯泡变暗,当烧杯中的Ba(OH)2完全反应后再加H2SO4,离子浓度又变大,灯泡又变亮 ③Ba2+与SO结合生成了BaSO4沉淀
(2)2H++SO+Ba2++2OH-===BaSO4↓+2H2O
-
题目来源: 山东省肥城市二中2016年高中化学
第二章《化学物质及其变化》综合检测题 新人教版必修1
试卷相关题目
-
16.某溶液中只含有K+、Fe3+、NO,已知K+、Fe3+的个数分别为3a和a,则溶液中K+与NO的个数比为( )
A.1︰2 B.1︰4
C.3︰4 D.3︰2
[解析] 溶液中正电荷数为3a×1+a×3=6a,由正负电荷守恒知NO的个数为6a。
[答案] A
-
17.(2015.重庆市杨家坪中学高一月考)常温下,在水溶液中发生如下反应
①16H++10C-+2XO===2X2++5C2+8H2O;②2A2++B2===2A3++2B-;③2B-+C2===B2+2C-。下列说法错误的( )
A.反应C2+2A2+===2A3++2Cl-可以进行
B.还原性由强到弱的顺序是C->A2+>B->X2+
C.氧化性由强到弱的顺序是XO>C2>B2>A3+
D.反应③是置换反应
[解析] 在一个确定的氧化还原反应中,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,由①16H++10C-+2XO===2X2++5C2+8H2O中,XO为氧化剂,C2为氧化产物,故氧化性:XO>C2;C-为还原剂,X2+为还原产物,故还原性:C->X2+;在②2A2++B2===2A3++2B-中,B2为氧化剂,A3+为氧化产物,故氧化性:B2>A3+;A2+为还原剂,B-为还原产物,故还原性;A2+>B-;在③2B-+C2=B2+2C-中,C2为氧化剂,B2为氧化产物,故氧化性:C2>B2;B-为还原剂,C-为还原产物,故还原性:B->C-;由上述分析知氧化性:C2>B2>A3+,故A中的反应可以进行,故A正确;由上述分析知还原性:A2+>B->C->X2+,故B错误;由上述分析知氧化性:氧化性由强到弱的顺序是XO>C2>B2>A3+,故C正确;反应③是单质C2与含B-的化合物的置换反应,故D正确。
[答案] B
[点评] 本题考查了氧化还原反应中氧化性还原性的比较,难度中等。做题时应注意分析三个反应中的氧化剂和还原剂,并且明确氧化性和还原性的比较规律。
-
18.亚硝酸盐中毒,又名乌鸦病、紫绀病、肠源性青紫病。亚硝酸盐可将正常的血红蛋白氧化成高铁血红蛋白,血红蛋白中的铁元素由二价变为三价,失去携氧能力,使组织出现缺氧现象。美蓝是亚硝酸盐中毒的有效解毒剂。下列说法中,不正确的是( )
A.在中毒过程中血红蛋白被氧化
B.中毒时亚硝酸盐发生氧化反应
C.药品美蓝应具有还原性
D.解毒时血红蛋白被还原
[解析] 本题考查氧化还原反应的应用。中毒过程中血红蛋白中的铁元素由二价变为三价,故血红蛋白被氧化,A项正确;中毒时血红蛋白发生氧化反应,则亚硝酸盐发生还原反应,B项错误;美蓝是亚硝酸盐中毒的有效解毒剂,因此美蓝能使高铁血红蛋白还原为正常的血红蛋白,即美蓝应具有还原性,C项正确;解毒时血红蛋白被还原,D项正确。
[答案] B
-
19.(2015.经典习题选萃)(7分)现有下列九种物质:①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)上述状态下可导电的是_________________________________________________;
属于电解质的是__________________________________________________________;
属于非电解质的是________________________________________________________。
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-===H2O,该离子反应对应的化学方程式为____________________________________________________________
________________________________________________________________________。
(3)⑨在水中的电离方程式为________________________________________________,
-
34.2 g ⑨溶于水配成250 mL溶液,SO的物质的量浓度为________。
[答案] (1)②⑦⑧⑨ ③⑤⑥⑨ ④
(2)Ba(OH)2+2HNO3===Ba(NO3)2+2H2O
(3)Al2(SO4)3===2Al3++3SO 1.2 mol/L
-
21.(2015.试题调研)(8分)如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
(1)请将分类依据代号填入相应的括号内:
( )两种物质都不是电解质
( )两种物质都是钠的化合物
( )两种物质都是氧化物
( )两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为_____________________________________________________。
②证明有红褐色胶体生成的实验操作是______________________________________
________________________________________________________________________。
[解析] (1)根据物质的交叉分类法可知H2和CO2都不是电解质,Na2O和NaCl都是钠的化合物,CO2和Na2O都是氧化物,NaCl和FeCl3都是盐。
(2)由红褐色胶体可知该胶体是氢氧化铁胶体,可通过丁达尔效应证明胶体的存在或生成。
[答案] (1)A C B D
(2)①FeCl3
②用一束光照射烧杯中的物质,若能产生丁达尔效应,则证明生成了Fe(OH)3胶体
-
22.(2015.四川省广安市高一期末)(9分)(1)下列物质能导电的是________;属于碱的是________;属于电解质的是________;(填编号)
①HCl气体 ②Ca(OH)2固体 ③KNO3固体 ④SO2 ⑤Cu ⑥氨水 ⑦KNO3溶液 ⑧石墨 ⑨蔗糖 ⑩硫酸钡固体
(2)某化学反应的反应物和产物如下:
Al+NaNO3+H2O―→Al(OH)3+N2↑+NaAlO2
a.该反应的氧化剂是___________________________________________________。
b.该反应的氧化产物是_________________________________________________。
c.反应过程中转移5 mol电子,生成标准状况下N2的体积为________L。
[解析] (1)水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质。①氯化氢气体只存在分子,故不导电,溶于水,能完全自身电离出自由移动的氢离子和氯离子,能导电,属于电解质;②Ca(OH)2固体为电解质,但没有溶于水或处于熔融状态,没有电离,故不能导电。③KNO3固体为电解质,但没有溶于水或处于熔融状态,没有电离,故不能导电。④SO2气体常温下为气体,只有SO2分子,没有自由移动的离子,不导电,SO2在水溶液中与水反应,生成亚硫酸,亚硫酸电离出自由移动的离子,溶液能够导电,但自由移动的离子不是SO2自身电离,SO2不属于电解质;⑤铜丝是金属单质,因为具有电子能导电,但它既不是电解质也不是非电解质;⑥氨水,有自由移动的离子能导电,它是氨气的水溶液,所以既不是电解质也不是非电解质;⑦KNO3在水溶液或熔融状态下都能够导电,属于电解质,但是KNO3溶液属于混合物,既不是电解质也不是非电解质;⑧石墨含有自由电子能导电,但石墨是单质,既不是电解质也不是非电解质;⑨蔗糖只存在蔗糖分子不导电,在水溶液中或熔融状态下都不能够导电,属于非电解质;⑩硫酸钡固体没有自由移动的离子不导电,在水溶液里或在熔融状态下,能完全电离出自由移动的钡离子和硫酸根离子导电,属于电解质。
(2)据方程式,Al元素的化合价从0价升高到+3价,失去3个电子,做还原剂;硝酸钠中氮元素的化合价从+5价降低到0价,得到5个电子,做氧化剂,水既不是氧化剂,也不是还原剂;氮气是还原产物,氢氧化铝和偏铝酸钠是氧化产物;每生成1 mol N2转移10 mol电子,转移5 mol电子,可生成0.5 mol N2即标准状况下的体积为11.2 L。
[答案] Ⅰ.⑤⑦⑧ ②⑥ ①②③⑩
Ⅱ.a.NaNO3 b.Al(OH)3 NaAlO2 c.11.2 L
-
23.(7分)(1)从下列各组反应对比中,判断哪种粒子的氧化性最强,哪种粒子还原性最强。
①铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质。则在Cu、Fe、Ag中,________的还原性最强;在Cu2+、Fe2+、Ag+中,________的氧化性最强。
②铁钉在氯气中被锈蚀为棕褐色物质(FeCl3),而在盐酸中生成淡绿色溶液(FeCl2)。则在氯气分子(Cl2)、氯离子、氢离子中,________具有氧化性,________的氧化性最强。
(2)为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:
KIO3+5KI+3H2SO4===3I2+3K2SO4+3H2O
①该反应中,氧化剂是______________,氧化产物是______________。
②当有3 mol I2生成时,有________mol还原剂被氧化。
[答案] (1)①Fe Ag+ ②Cl2、H+ Cl2
(2)①KIO3 I2 ②5
-
24.(7分)有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是________,一定不含的物质是________,可能含有的物质是________。(以上各种物质均写化学式)
(2)写出下列步骤中发生反应的离子方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
[解析] 混合物溶于水后产生白色沉淀,形成的滤液呈无色,说明溶液中没有Cu2+,原粉末中肯定无CuSO4。根据题意,沉淀物一定是BaCO3,说明固体粉末中有Ba(NO3)2和Na2CO3;但依据滤液与AgNO3溶液作用产生白色沉淀,这种白色沉淀可能是AgCl沉淀,也可能是Ag2CO3沉淀,故无法判断原白色粉末中是否存在NaCl。
[答案] (1)Ba(NO3)2、Na2CO3 CuSO4 NaCl
(2)Ba2++CO===BaCO3↓
BaCO3+2H+===Ba2++CO2↑+H2O
SO+Ba2+===BaSO4↓


